饮用水,生活污水和工业废水的分析
(一)饮用水分析
1. 卤素含氧酸的测定
饮用水用氯气消毒,因其成本低,消毒效果较好而得到广泛的使用。但自1970 年以来的研究表明,在使用氯气消毒的过程中可能会产生致癌的副产物如三卤甲烷,因此各国正在寻找一种更为安全可靠的可替代氯气的消毒方法。目前发达国家较为普遍的是使用二氧化氯和臭氧作为饮用水和水箱贮水的消毒剂。研究表明,上述消毒剂在使用过程中也会产生少量对健康不利的副产物如,亚氯酸根,氯酸根和溴酸根。使用二氧化氯溶液对饮用水进行消毒时可以伴随生成亚氯酸根(ClO2-)和氯酸根(ClO3-)。用次氯酸盐(如漂白粉)溶液消毒,会将氯酸根引入末级处理后的饮用水中。而用臭氧对饮用水消毒的过程中会将水体中自然存在的溴化物氧化为对人体有害的溴酸根。
作为ClO2 消毒剂的副产物,已经有不少的报道对ClO2- 和ClO3-进行了研究。使用二氧化氯对饮用水消毒时,二氧化氯溶于水,生成亚氯酸和氯酸
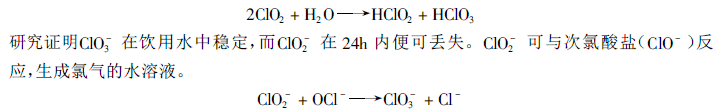
饮用水中经常需要测定的离子包括常见的阴,阳离子和消毒剂的副产物如一些卤素含氧酸:亚氯酸根(ClO2-),次氯酸根(ClO-),氯酸根(ClO3-),溴酸根(BrO3-),溴化物(BrO-)等。美国国家环保局(EPA)已经建议使用化学抑制型离子色谱法测定上述含氧卤素副产物。在水处理过程中,二氧化氯的用量很少,因此水中反应副产物亚氯酸根和氯酸根的浓度通常比较低。hautman和Bolyard研究了在干扰离子Cl- 、CO32-和NO3-存在的情况下用四硼酸钠 - 硼酸淋洗液分离卤素含氧酸的方法。使用电导和紫外检测器进行测定,方法的最低检出限为10μg/L。采用高容量的阴离子分离柱如Dionex公司的IonPacAs9HC型阴离子分离柱,在大量常见阴离子的存在下,一次进样可分离多种含氧卤素和其他的常见阴离子。图8-6-1 为用AS9HC型阴离子分离柱测定模拟饮用水中μg/L级含氧卤素和溴离子。
用大体积进样直接测定饮用水中低浓度卤素含氧酸和溴酸盐时,为使基线噪音处于较小的状态,开机后仪器的稳定时间要稍长,以使背景电导达到稳定状态。基于上述原因,在允许的情况下,应尽量让仪器连续运行。使用IonPacAS-9HC阴离子分离柱、淋洗液为9mmol/LNa2CO3 时,达到平衡后其背景电导应在20-24μs之间。另外,实验表明,使用外加水方式比自动再生方式的背景电导要低。实验证明,在不影响BrO3- 与Cl- 分离的情况下,500μl是最大可允许的进样量。当注入750μl时,离子交换基团过载BrO3-与Cl- 发生共淋洗。
虽然溴酸盐在饮料和面包制造业已使用了许多年,但近年来的研究证明溴酸根是一种潜在的致癌物质。由于臭氧可将饮用水中的溴离子氧化为对人体健康有影响的溴酸根而引起人们的关注。世界卫生组织建议饮用水中溴酸根的含量应控制在25μg/L 以下。美国EPA则要求用臭氧处理的饮用水中溴酸根的浓度应<10μg/L。

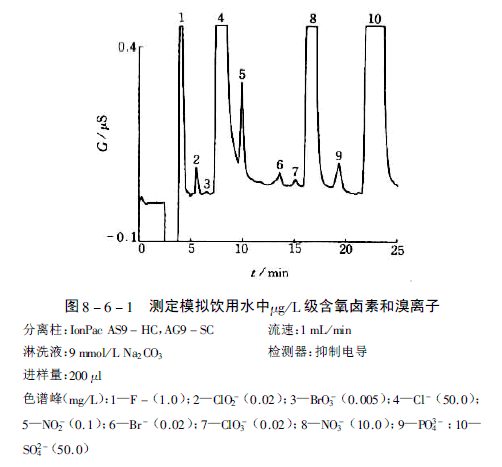
臭氧将Br-通过其中间体OBr- 氧化为BrO3-。从反应方程式中也看到,臭氧并没有将次溴酸(HOBr)氧化为溴酸根。由于增加的酸(H3O+ )有利于生成次溴酸,在低Ph条件下的臭氧化作用则不利于溴酸根的生成,参见图8-6-2。
Hautman等用IonPac AS9 -SC分离柱;硼酸淋洗液;200μl进样量直接测定了饮用水中的溴酸根,最低检出限为7.3μg/L。此检出限接近典型的臭氧化水样中溴酸根的浓度。
Joyce等人提出了一种更灵敏且与ASTM方法一致的测定溴酸根的方法。在该方法中,首先对样品进行了保护性处理。即用惰性气体或高纯氮气通入样品中(5min)除去残留的二氧化氯或臭氧。为防止次溴酸根被转化溴酸根,样品中加入乙二胺(1ml/L)使其生成溴胺。由于样品中存在大量的常见阴离子如SO42-、CO32-等,特别是氯离子其浓度一般较溴酸根的浓度高3 个数量级以上,须将样品通过可以消除上述干扰离子的前处理柱,例如Dionex公司的OnGuard-Ba,OnGuard-Ag,和OnGuard - H。使其分别生成硫酸钡、氯化银沉淀,并将碳酸根转化为碳酸。研究证明,为使硫酸根完全沉淀,样品中应加入有足够浓度的二价阳离子以置换树脂上的二价钡离子,使之能与硫酸根进行反应。实验结果表明,120mg/L 镁离子(氯化镁)从钡型交换树脂上置换的钡离子可除去500mg/L 硫酸根。该方法的最低检出限在进样体积为5ml时可以达到1μg/L 以下。此外,为防止银型预处理柱上的银离子玷污浓缩柱和分离柱,应在进样阀与浓缩柱之间安装一支装有螯合树脂的短柱以吸附漏出的银离子。
2. 饮用水中亚硝酸盐、硝酸盐的测定
饮用水中亚硝酸盐、硝酸盐是必测项目之一。亚硝酸钠和亚硝酸钾在食品生产中广泛用作防腐剂和颜色的固定剂。亚硝酸盐是氮循环中的一种中间状态,存在于土壤、水体和废水中。在工业上,亚硝酸盐用来抑制工业用水的腐蚀作用。近年来人们已经注意到亚硝酸盐在胃里可与胺类和酰胺类化合物生成致癌性很强的亚硝胺化合物。
常见的测定亚硝酸盐的方法有滴定法,分光光度法和电位滴定法等。近年来,离子色谱法正逐渐代替上述湿化学法而成为一种常规的分析方法。
因为亚硝酸盐易被氧化为硝酸盐,因此,测定亚硝酸盐的样品不应放置过长。在样品分析中,亚硝酸盐的含量一般较低,如饮用水中通常仅为几个μG/L,而其他的阴离子如Cl- 和SO42-等的含量往往高出4-5 个数量级,特别是保留时间小于亚硝酸盐的氯离子含量高时会使低含量的亚硝酸盐保留时间提前并会对其有“遮盖”作用,而自来水中由于消毒等原因,氯离子的含量通常大大高于亚硝酸盐浓度。因此,要定量测定水中微量的亚硝酸盐除了选用柱容量较大的分离柱外,还可以采用以下方法。
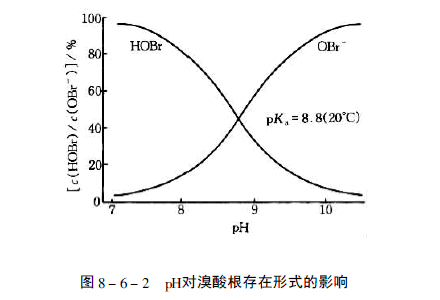
(1)化学抑制型离子色谱,使用紫外检测器由于氯离子在紫外区域吸收较弱而亚硝酸盐和硝酸盐在210nm有较强的吸收,因此可以使用紫外检测器测定亚硝酸盐和硝酸盐。仪器连接的方法是将分离柱出口处直接连接到紫外检测器的入口。欲同时测定其他阴离子,则系统流路可按图8-6-3 所示联接,同时使用电导和紫外两种检测器。
用紫外检测器,于波长210nm处测量,25μl进样量,对NO2-的最低检出限为10μg/L,NO3-为15μg/L。以NO2- —N 计为3.0μg/L,以NO3-—N 计为3.5μg/L。方法对(NO2-)线性范围是10μg/L - 50mg/L ,对(NO3-)的线性范围是15μg/L-75mg/L。
(2)样品前处理最简单的前处理方法是稀释,但稀释后微量的亚硝酸根离子更加难以测定。采用离子交换树脂处理样品是一种简单可行的方法。Ag型离子交换树脂可以除去样品中的氯离子。氯离子进入柱内与银离子生成氯化银沉淀:Ag++Cl-→AgCl↓。目前,该类产品在市场上有多家公司的产品有售,例如前面提到的OnGuard - Ag预处理柱。也可以自行制备前处理柱。
(二)生活污水和工业废水分析
1. 多聚磷酸盐的测定
有机磷和多聚磷酸盐是常用的化学添加剂。由于Ca2+ ,Mg2+ 与多聚磷酸盐有较强的络合能力,所以工业中广泛用多聚磷酸盐作为循环水中的阻垢剂和防蚀剂;日用化学品如洗涤剂、牙膏等加入多聚磷酸盐以软化硬水。
大量的磷酸盐排入水体中极易引起水体的富营养化,使得水中水生植物大量繁殖,消耗氧分,导致水生生物的死亡。目前许多发达国家已禁止使用多聚磷酸盐做化学添加剂。
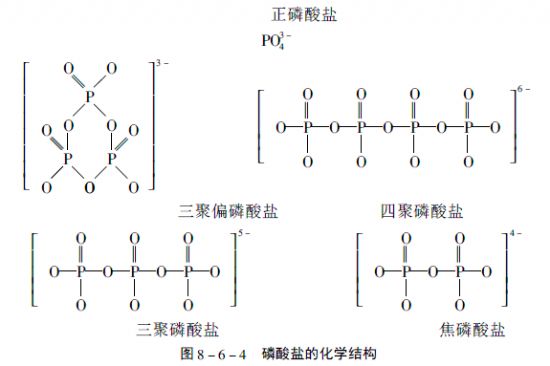
对多聚磷酸盐的分析如P2O75-,P3O105-,一般是先将其转化为PO43-用光度法测定总磷,此法不仅要作样品前处理,而且不能进行形态分离。
用离子色谱法,阴离子交换分离;氢氧化钠淋洗液和甲醇有机改进剂,梯度淋洗分离多聚磷酸盐(正磷酸盐PO43-、焦磷酸盐P2O74-、三聚磷酸盐P3O105-),化学抑制电导检测的最低检出限达到15-50μg/L。
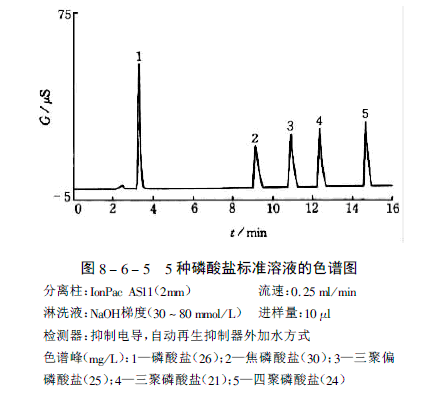
近来使用疏水性非常低的阴离子分离柱分离多聚磷酸盐有了新的进展。一次进样可同时测定正、焦、三聚和四聚磷酸盐。图8-6-4为磷酸盐的化学结构;图8-6-5 为同时分离5种磷酸盐的标准色谱图。
2. 铬的测定
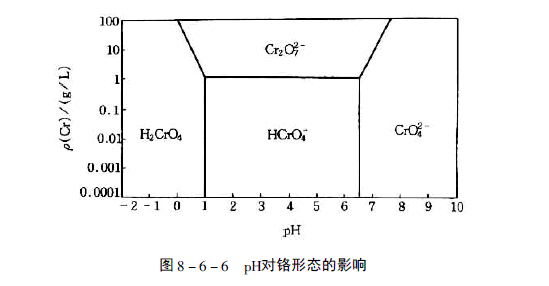
铬在环境中主要是以三价Cr(Ⅲ)和六价Cr(Ⅵ)的形式存在。其中三价铬由于其配位体交换动力学缓慢,反应活性较低,对生物体的毒性轻微。对于哺乳类动物,三价铬是维持其体内葡萄糖、脂类和蛋白质代谢的基础。六价铬的毒性大,其存在形式依据?9的不同主要为铬酸(H2CrO4)及其盐(HCrO4-)和铬酸根离子(CrO42-)3 种。pH<1 时以H2CrO4为主要形式;pH在1-6 之间时以HCrO4-为主;pH=6 以上时以CrO42-为主,见图8-6-6。
重铬酸盐CrO42-实际上是失去一个水分子的HCrO4-的二聚物,当铬的浓度超过大约1g/L时生成。六价铬是一种强氧化剂,其氧化能力是pH的函数。pH值下降时,Cr(Ⅵ)的氧化性增强。由于环境样品通常为碱性,而且Cr(Ⅵ)的还原电位随着pH值的增加而下降,Cr6+ 的氧化性大大降低。
六价铬对动物的肺、肝和肾等脏器有伤害作用并对皮肤有刺激性,可以使皮肤发生溃疡,已确认为致癌物,且能在体内蓄积。含有铬的化合物广泛用于电镀、制革、纺织、造纸、染料工业中,这些企业排放的工业废水中可能会含有对环境有污染的铬类化合物。因为Cr3+对环境的影响远没有Cr(Ⅵ)那样大,因此人们对铬的关注主要集中在Cr(Ⅵ)的测定方面。测定铬的最经典方法是二苯碳酰二肼比色法。二苯碳酰二肼在酸性条件下与六价铬作用,生成一个紫红色的络合物,在可见光区有强的吸收。
离子色谱法是近年来新发展的一种灵敏高、选择性好的测定铬的分析方法,一次进样可同时测定Cr3+ 和Cr(Ⅵ)。测定环境样品中铬的研究工作已有报道,并且一些机构已将此法作为标准方法或推荐方法供使用执行,例如测定大气颗粒物中和废弃物焚化炉排放的气体中的六价铬。有报道用IC-ICP-MS,-连用技术同时测定Cr3+ 和Cr(Ⅵ),最低检出限分别可达到8.1×10-5和8.8×10-5mg/L Cr。
六价铬的离子色谱法分析:用阴离子交换分离柱,(例如Dionex的IonPacas7阴离子分离柱),淋洗液为硫酸铵5 氢氧化铵。分离后Cr(Ⅵ)与柱后衍生试剂二苯碳酰二肼(DPC)产生如下反应:
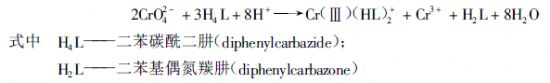
上述反应中,二苯碳酰二肼被氧化为二苯基偶氮羰肼(diphenyl - carbazone),Cr(Ⅵ)被还原为Cr3+;Cr3+ 与二苯基偶氮羰肼螯合生成一个目前结构尚不清楚的紫色络合物,于波长520nm处测定。
三价铬和六价铬的同时测定:先用氢氧化钠和盐酸调节样品pH至6.8,然后向100ml锥形瓶中加入10ml浓10 倍的淋洗储备液(20.0mmol/L PDCA,20mmol/LNa2PO4,100mmol/LNal,500mmol/LCH3CO2NH4,28.0mmol/L LiOH和10ml样品。加热至沸腾,保持1min。待样品冷却至室温后用去离子水稀释至100ml。
在使用PDCA(吡啶2,6 - 二羧酸)淋洗液时,由于Cr3+ 的配位体交换动力学速度较慢,因此在柱前与PDCA反应生成一价阴离子络合物Cr(PDCA)2-。其柱前衍生反应步骤如下:六价铬不与PDCA反应,在近中性的PDCA淋洗液中以两价阴离子CrO42-形式存在。一价阴离子络合物Cr(PDCA)2-和二价阴离子CrO42-经阴离子交换分离后,Cr(Ⅵ)通过柱后衍生形成Cr(Ⅵ)- DPC络合物(于520nm#测量),进样量为250μl时,Cr3+和Cr(Ⅵ)的最低检出限分别为30μg/L和0.3μg/L,其标准溶液的色谱图见图8-6-7。

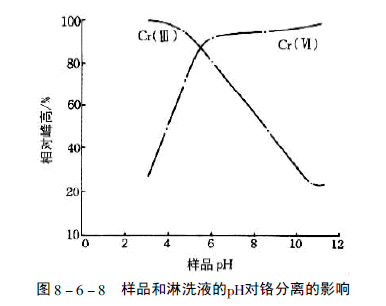
样品和淋洗液的pH对分离结果有较大的影响。如图8-6-8所示,pH=6 或更高时,将不利于Cr(PDCA)2-配合物的生成。pH>8 时,Cr(Ⅵ)以CrO42-为主;pH<6 时,CrO42-开始转化为对色谱柱有害的Cr2O72-。为优化分离与检测Cr3+ 和Cr(Ⅵ)的色谱条件,系统和样品的pH选择6.8 为宜。
分析含铬样品时,除了选择适当的色谱条件外,样品前处理亦十分重要。采集含铬的样品须用茶色玻璃瓶。使用前用(1+1)HNO3 清洗,然后用去离子水冲洗干净。在采样和样品制备过程中常常要加入酸或碱改变样品的!"。如前所述,在分析多价态的样品时,pH的改变可能会使样品中各氧化态的相对浓度起变化,应根据测定的对象慎重处理。为了保持样品的原貌与完整性,所采集的样品应置于冷藏箱内保存,并尽量减少对样品的处理。分析饮用水、雨水和空气提取液时,样品可在通过0.45μm滤膜过滤后直接进样而无须做其他前处理。
3. 水体中重金属离子的测定
离子色谱分析金属离子时,其突出的优点是可检测元素的不同氧化态,例如Fe2+, Fe3+ ,Cr(Ⅲ)/Cr( Ⅵ)和Sn(Ⅱ)/Sn(Ⅳ)等,以及一次进样同时分析多元素。离子色谱在线浓缩富集和基体消除技术有力地解决了基体干扰和检测灵敏度等关键问题。因此,对于研究金属的生物利用度,以及对环境的影响,离子色谱是一种非常有用的手段。
离子色谱分离金属离子的方法是基于阳离子交换的可逆络合反应和阴离子交换的不可逆络合反应。阴离子交换具有选择性较好,且适于分离复杂样品的优点。Nicola等人使用了一种新型的混床离子交换柱测定了污水处理厂水样中的过渡金属。
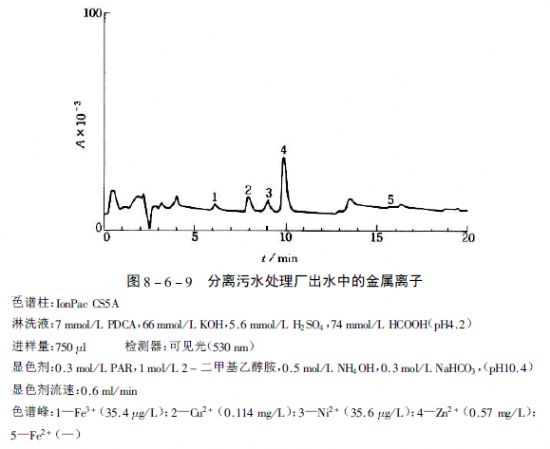
图8-6-9 为污水处理厂出水水样中金属离子的色谱图。在进行分析前,对所分析的污水样品在进样前先用6mol/L HCL酸化到pH2,过滤,用去离子水1:10(V /V)稀释。
4. 氰化物
作为一种添加剂,许多工业的生产过程需要使用氰化物,例如金属电镀、钢和贵金属的淬火等。氰化氢常用于聚丙烯腈塑料的生产。对矿石中的黄金进行湿法冶金萃取时需要使用氰化钠(氰化作用)。氰化作用的过程中,将会使许多金属离子与氰离子生成金属氰络合物。所生成的这些络合物大部分是非常稳定的,浓度也比氰化金高。
在高温下,聚丙烯腈塑料分解会产生致命的氰化氢。氰化过程中排放的废水如果没有经过处理直接排放将会对环境和水生生物造成严重的危害。为保护环境资源的可持续利用,各国对环境各种载体中氰化物的浓度都有严格的规定。例如国家环保局规定地表水中氰化物的含量不得超过3.5μg/L。世界卫生组织标准对饮用水允许的浓度是50μg/L,而美国的NIOSH规定空气中氰化氢可允许的浓度为5mg/m3。人类可能受氰化物玷污的途径有吸入、摄取和皮肤吸收等。因此,严格控制和监测环境中氰化物的浓度是十分必要的。
关于氰化物样品采集、分析方法的综述最初是由NIOSH1976 年发表的。这些方法包括了比色、滴定、气相色谱、原子吸收和红外吸收光谱。近年来,离子色谱法应用于各种复杂基体中氰化物测定的报道正在增加,其中Out较为全面地叙述了离子色谱法分析氰化物和金属氰化物所取得的进展。与其他分析手段相比,如比色法,在样品有较高的基体存在时,离子色谱在消除干扰,定量的准确性方面要优于前者。美国材料与试验协会(ASTM)已将离子色谱法确定为测定水中氰化物的标准分析方法。
样品中的总氰是指游离氰(包括CN- ,HCN和部分在弱酸性的溶液中能快速离解的与Ag,Cd,Cu,Ni和Zn生成的络合氰)和络合氰(有较高稳定常数的与An,Co,Fe,Hg,Pd和Pt生成的络合氰)两大类。测定样品中的总氰需要先将样品置于沸腾的浓硫酸中进行消解蒸馏,氰化物、游离或络合的金属氰化物以氰氢酸气体的形式释放,如下式:

然后用光度法或离子色谱法分析吸收液中的氰化物。从以上反应中可见,若样品中含有硫化物,消解蒸馏时硫离子也会释放出来,并被碱性溶液吸收。
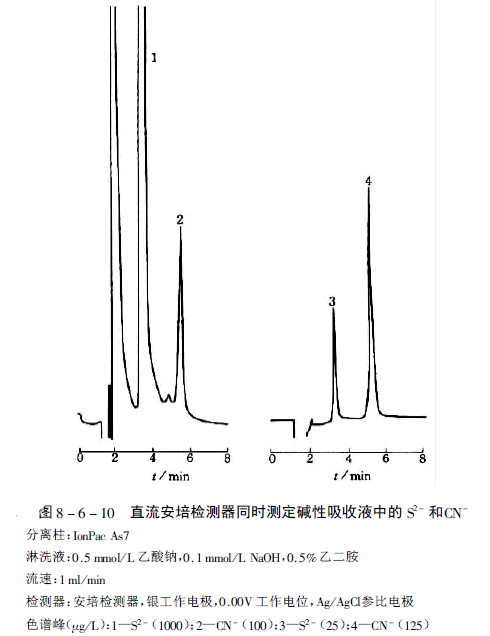
常用测定氰化物的各种湿化学法,如比色法,各种电化学法等,其共同的缺点是易受干扰。例如比色法测定氰化物时,样品中存在的硫化物,硫氢化物和游离氰基团中的金属氰化物对比色法有干扰。硫化物对离子色谱法无干扰,并且可以同时测定CN- 和S2- 。图8-6-10是用直流安培检测器同时测定碱性吸收液中的S2- 和CN- 的色谱图。
安培检测器对氰化物有较高的灵敏度,如进样量150μl,可以测出5μg/L 的Au(CN)2-。
测定氰化物的方法可分为直接法和间接法两种。直接法多使用安培检测器直接测定溶液中的氰化物;间接法则多使用UV检测器。相比较而言,安培检测器的灵敏度要高一些。
【直接法】
氰化物在银电极上有较强的电化学活泼性,直接监测灵敏度可以达到μg/L 范围。将安培和电导检测器串联使用同时测定了“游离”的和“不稳定”的氰化物,硫化物和卤素离子。将电化学检测器置于分离柱和抑制器之间,而将电导检测器置于抑制器之后。用阴离子分离柱,pH=11.0的淋洗液(色谱条件见文献),在进样量100μg/L时,CN- 的最低检出限为2μg/L。在此色谱条件下,Cd,Zn与氰化物的络合物解离,并以游离氰的形式被测定。Ni和Cu与氰生成的络合物解离缓慢,造成峰拖尾。An,Fe和Co与氰生成的络合物在此色谱条件下不解离,全部保留在色谱柱内。
经光化学辐射之后,将φ=3%次磷酸加入解离的金属氰络合物中,Pohlandt用安培检测器测定了总氰,所使用的淋洗液与Rocklin和Johnson使用的相同。
Koch提出了一种用阴离子分离柱分析空气和尘埃中Cn- 的方法。样品收集在一块干燥的实验室用吸收织物上,采集后用淋洗液超声波萃取。淋洗液除了5mmol/L NaOH外,其余与Rocklin和Johnson相同。用安培检测器检测,CN-的检出限为1μg/L,硫化物不干扰。
Mehra和Franhenberger报道用Vydac302 离子色谱柱,5mmol/L 邻苯二甲酸氢钾(pH=4.3)淋洗液,安培检测器同时测定湖水中的CN-,Cl-,Br- 和I- 。方法的检出限是0.2-12μg/L,回收达到95%-105%。Jandik用Waters公司的IC - Pak阴离子柱,5.0mmol/L KOH淋洗液和安培检测器测定了土壤样品中的氰化物,检出限为100mg/L。在另一项河流和沼泽的研究中,Jandik等人也使用了安培检测器和Waters的IC -Pak阴离子分离柱和两种淋洗液:2mmol.L邻苯二氢钾(KHP),5mmol/L KOH或5mmol/L磷酸,方法的检出限为2μg/L。
Imannan等人用东洋曹达公司(TSK)GEL IEX 520 QAE硅胶型离子交换柱分离氰化物及[Fe(CN)6]4- 和[Fe(CN)6]3- 。该方法以0.05mol/L Fe(ClO4)3和0.8mol/L HClO4 为柱后衍生试剂,于ML340nm紫外检测。氰化物检测的灵敏度达到0.16μg/L。
【间接法】
pKa小于7 的阴离子可直接用电导测定。HCN是一种弱酸,离解常数pKa为9.3不宜用电导直接测定,已经有若干间接测定的方法被报道。Hisayuki7报道了一种用离子色谱间接测定氰化物的方法。方法的原理是在预处理柱内让CN- 和Agl反应生成I- 。使用阴离子分离柱,2.2mmol/L Na2CO3淋洗液,用次氯酸盐将天然水和废水中的游离氰和金属氰化物氧化为氰酸盐(pKa=3.66)后进行测定。将CN-(金属键)氧化为CNO- 的氧化反应不能够使氰与Fe,Au和Co的络合物离解,甚至温度提高到80℃也无法使它们离解。
5. 金属氰络合物
已报道测定金属氰络合物的方法有离子交换和离子对色谱法。检测方法一般使用UV或电导检测器。上述分离方法中,由于金属氰化物对离子交换树脂有很高的亲和力,将其洗脱需要较长的时间,同时所使用的淋洗液对人体有毒害作用,因此此类方法已经被更快速,便捷的离子色谱法所取代。Out等用表面疏水性较低的阴离子分离柱(AS5),梯度淋洗,从Ag(CN)2-,Cu(Cn)43-,Ni(CN)42-,FE(CN)63-和Co(CN)63-络合物中分离了Au(CN)2-使用UV检测器(215nm),进样量为150μl,对Au(CN)2-的最低检出限为5μg/L。
Haddad等人用离子对色谱法在Waters的IC Nova Pak C18和CN柱上测定金属氰络合物。在该方法中,首先在C18预柱上富集2ml浓度分别为Au10μg/L,CN-100μg/L 的样品,然后用UV检测器于215nm波长测定。Au的检出限为0.43μg/L。所用淋洗液是5mmol/L 四丁基氢氧化胺- 甲醇(体积比68:32)。预富集方法也曾用于测定Pb(Ⅱ),Pb(CN)42-和Pt(CN)42-金属氰络合物。同时在实验中观察到,所富集样品的体积对样品的回收率能产生较大的影响。当样品的体积增加时,回收率下降。对这种现象的解释可能是离子对试剂解析或者由于氰化物阴离子(CN- )竞争交换位置所造成的。

