颗粒内熟化助力“量子点纳米晶分子”探针的精准合成
癌症目前已经成为全球发病率最高的疾病之一,正严重威胁着人类的健康发展。光学成像技术,因其在监测肿瘤微环境、病灶的发生、转移等相关过程的优异特性,而广受关注。其中基于近红外的活体成像,因其低的背景干扰以及组织散射和吸收,表现出了巨大的应用前景。此外,近几年通过纳米晶的耦合杂化技术来调控纳米晶之间的耦合杂化作用,为近红外响应型分子探针的制备提供了新的研究思路。
胶体半导体量子点由于小尺寸效应,其能态分布处于分子态和固态之间,通常被称为“人造原子”。受原子杂化耦合构建分子的启发,以色列希伯来大学(Hebrew University of Jerusalem)的Uri Banin教授团队近年来在量子点耦合探针的制备领域取得了一系列开创性的成果(Angew. Chem. Int. Ed., 2021, 60, 14467-14472; Acc. Chem. Res., 2021, 54, 1178-1188; Nat. Commun., 2019, 10, 5401)。这类新型耦合量子点纳米晶分子探针在传感、活体成像、光电以及量子通讯技术等方面具有优异的应用前景。
目前纳米晶分子晶体的精准可控制备以及相关形成机制的研究,仍然面临着巨大的挑战。最近崔家斌博士等以胶体半导体量子点这种“人造原子”作为构建纳米晶分子的结构基元,通过调控配体浓度、反应温度等变量因素,精准控制量子点纳米晶耦合杂化,同时结合纳米晶颗粒内熟化策略,制备出不同性质的耦合红移响应型“耦合型纳米量子点分子”(图1)。
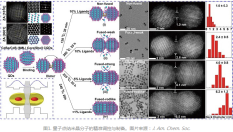
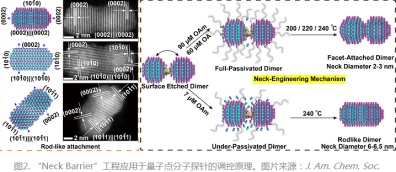
通过“Neck Barrier”工程,研究人员实现了从量子点耦合二聚体到耦合纳米棒分子的精准调控(图2)。同时研究人员发现,减少配体浓度以及升高融合温度,将使得量子点表面不能充分钝化,导致了纳米晶颗粒之间的熟化,促使表面原子迁移速率加剧,并填充在缺陷和应力大的耦合界面处,形成了形貌可控的量子点纳米棒分子结构,增强了二聚体之间的耦合杂化,实现了分子探针的吸收光谱以及荧光发射光谱的显著红移。总而言之,颗粒内熟化与纳米晶耦合技术的结合,为生物成像纳米探针的设计以及癌症的精准治疗与诊断提供了可行的研究方案。
该工作近期发表在美国化学会化学旗舰刊J. Am. Chem. Soc.上。文章第一作者为崔家斌博士。
来源:X-MOL

